SMA : la thérapie génique arrive pour les plus de deux ans aux États-Unis
C’est sous le nom d’Itvisma que le produit de thérapie génique, administré par une injection intrathécale unique, sera disponible uniquement pour les plus âgés dès le mois de décembre 2025 sur le territoire américain.
Un même produit, deux noms de médicaments
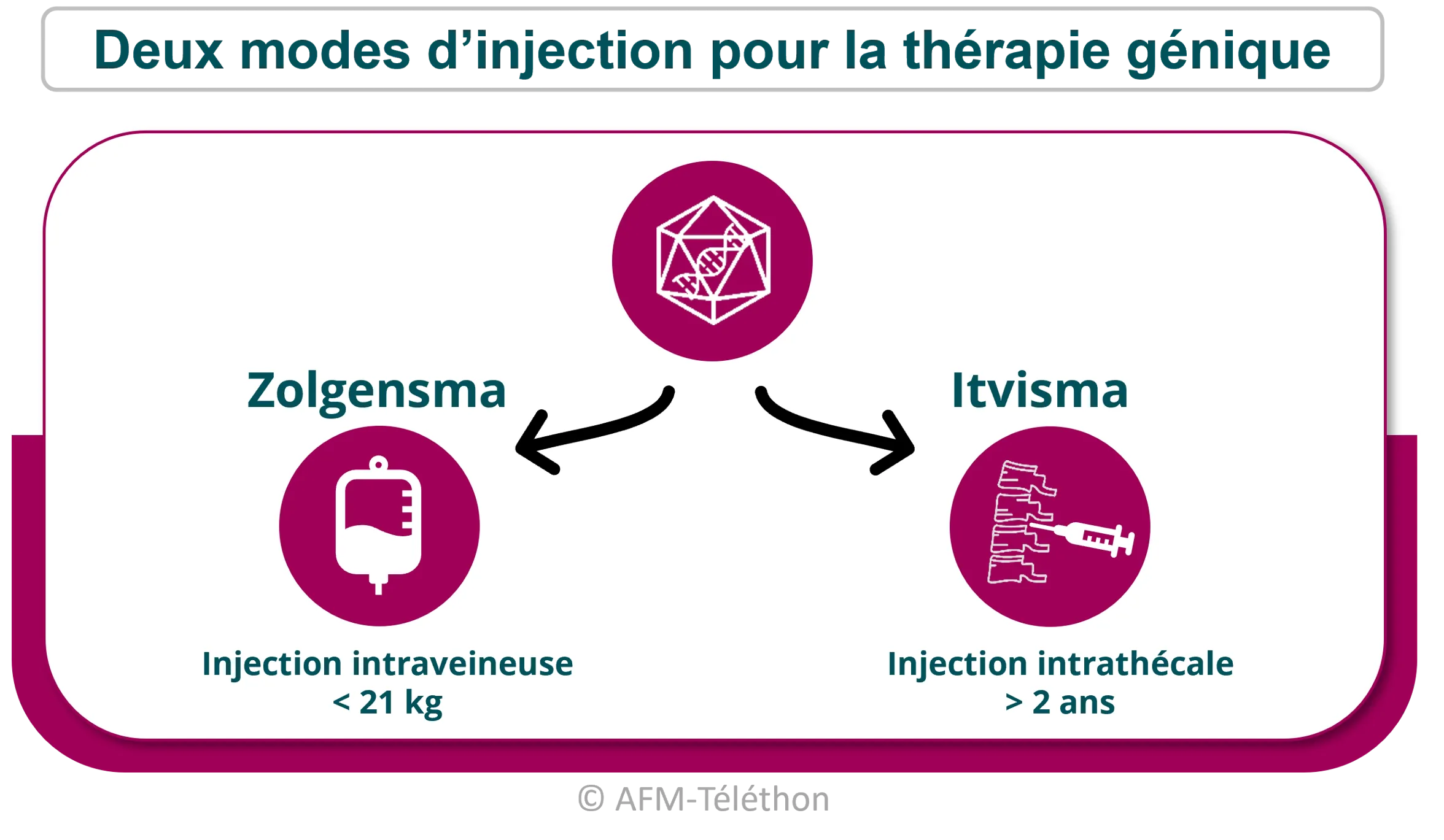
Le produit de thérapie génique Zolgensma développé par Novartis s’adresse aux enfants pesant moins de 21 kg. Il est administré lors d’une perfusion intraveineuse unique.
Suite aux résultats positifs sur la fonction motrice de deux essais cliniques de phase III (les essais STRENGTH et STEER) menés chez des patients plus âgés (âgés de 2 à 18 ans), les autorités de santé américaines viennent d’annoncer l’autorisation du produit de thérapie génique disponible à partir de l’âge de deux ans, cette fois sous le nom d’Itvisma. Pour plus d’efficacité, il est administré en une injection, par voie intrathécale (entre deux vertèbres lombaires) afin de mieux cibler les motoneurones de la moelle épinière.
Et en Europe ?
Le dossier de demande d’autorisation de l’Itvisma est en cours d’analyse par les autorités de santé européennes qui devraient rendre leur décision en milieu d’année 2026. Si l’avis est positif, le dossier sera ensuite étudié par les autorités de santé de chaque pays d’Europe pour décider des conditions d’accès à ce nouveau médicament.
Source
Novartis receives FDA approval for Itvisma®, the only gene replacement therapy for children two years and older, teens, and adults with spinal muscular atrophy (SMA). Novartis. Communiqué de presse du 24 novembre 2025.
